 |
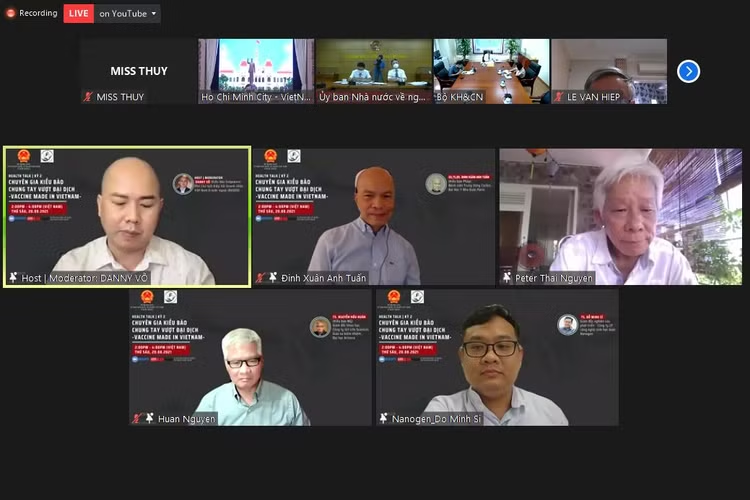
| Các chuyên gia đóng góp ý kiến tại Toạ đàm trực tuyến "Chuyên gia kiều bào chung tay vượt qua đại dịch" tổ chức chiều 20/8 |
Để khắc phục tình trạng khan hiếm vắc xin phòng ngừa Covid-19 ở phạm vi toàn cầu và đáp ứng nhu cầu cấp bách phòng chống dịch trong nước, giới khoa học và doanh nghiệp trong nước đã và đang rất nỗ lực nghiên cứu, sản xuất vắc xin để phấn đấu đưa vào sử dụng, tiêm chủng cho người dân trong năm nay. Trong số các sản phẩm đang được nghiên cứu, thử nghiệm, vắc xin Nanocovax của Công ty CP Công nghệ sinh học dược Nanogen đã bước vào thử nghiệm giai đoạn 3, vắc xin Covivac của Viện Vắc xin và Sinh phẩm y tế Nha Trang (IVAC) đang thử nghiệm giai đoạn 2, vắc xin ARCT-021 của VinBiocare (thuộc Tập đoàn Vingroup) đang thử nghiệm giai đoạn 1...
Theo TS. Đỗ Minh Sĩ, Giám đốc Nghiên cứu phát triển Công ty CP Công nghệ sinh học dược Nanogen, Công ty đã gửi Bộ Y tế báo cáo dữ liệu thử nghiệm lâm sàng giai đoạn 3a để các chuyên gia phân tích, đánh giá. Đây là báo cáo giữa kỳ pha 3 có ý nghĩa rất quan trọng để xem xét khả năng được cấp phép sử dụng khẩn cấp hay không?
Để nhanh chóng thoát ra khỏi đại dịch, theo TS. Nguyễn Hữu Huân - Giám đốc khoa học Công ty IGY Life Sciences (tại Hoa Kỳ và Canada), giáo sư kiêm nhiệm Đại học Arizona, việc cấp phép khẩn cấp vắc xin phòng Covid-19 made in Vietnam là điều nên làm lúc này.
Theo TS. Nguyễn Hữu Huân, để có thể được cấp phép sử dụng khẩn cấp, vắc xin phòng Covid-19 phải đáp ứng được 4 điều kiện, gồm: tính an toàn (quan trọng nhất), hiệu quả, khả năng sản xuất và lợi ích.
Theo đó, vắc xin Nanocovax đáp ứng được 4 điều kiện này. Nanocovax sử dụng công nghệ Protein tái tổ hợp, tạo kháng thể trung hòa, nhà sản xuất có sinh phẩm dùng để truyền tĩnh mạch (tinh khiết, có chất lượng cao) và có khả năng mang lại lợi ích lớn.
Cụ thể, về tính an toàn, Nanocovax là vắc xin chỉ cho hệ miễn dịch tiếp xúc với một thành phần duy nhất là phân tử gai (spike protein) của virus SARS-CoV2 để cơ thể tạo ra kháng thể bảo vệ (giống vắc xin mRNA của Moderna hay Pfizer), không gây áp lực cho tế bào. Trong khi đó, các vắc xin dùng công nghệ Adenovirus như AstraZeneca, J&J, Sputnik V thách thức hệ miễn dịch bởi các thành phần khác của adenovirus (khoảng 15 proteins chính). Trên thực tế, một số vắc xin dựa trên công nghệ này như vắc xin viêm gan B, cúm, Novavac (Covid-19)... đã chứng minh được độ an toàn.
Về hiệu quả, các vắc xin Covid-19 đang được sử dụng trên thế giới đều cho thấy kết quả thử nghiệm lâm sàng giai đoạn 3 phù hợp với kết quả giai đoạn 1 và 2 (tác dụng bảo vệ liên quan trực tiếp đến kháng thể trung hòa). Kết quả thử nghiệm giai đoạn 2 của Nanocovax đã cho thấy vắc xin này tạo kháng thể trung hòa tốt. Mức độ bảo vệ tỷ lệ thuận với lượng kháng thể trung hòa. Lượng kháng thể trung hòa do Nanocovax tạo ra cao hơn so với lượng kháng thể ở người nhiễm Covid-19 đã hồi phục, tương tự như vắc xin Moderna.
Về khả năng sản xuất, Nhà sản xuất đã có những sản phẩm sinh học dựa trên công nghệ tái tổ hợp dùng để tiêm tĩnh mạch. Đây là những sản phẩm đòi hỏi chất lượng và độ tinh khiết rất cao nên có thể sản xuất được vắc xin đảm bảo chất lượng.
Về lợi ích, trước tình trạng dịch bệnh căng thẳng hiện nay, việc cho phép sử dụng khẩn cấp vắc xin Nanocovax là cơ hội thành công cho Việt Nam trên lĩnh vực tự sản xuất được vắc xin và tự khống chế được đại dịch. Việc sử dụng đại trà vắc xin này tại thời điểm hiện hay có rủi ro rất nhỏ. Nếu có, theo lý thuyết, thì rủi ro sẽ thấp hơn so với các vắc xin đang được lưu hành nhưng lại có lợi ích rất lớn. Trước đây, Việt Nam cũng đã tự nghiên cứu, sản xuất và sử dụng vắc xin tả (ý tưởng của cố GS.TS Đặng Đức Trạch) nên đã khống chế được đại dịch và hiện nay vắc xin tả được sử dụng ở nhiều quốc gia trên thế giới dựa trên nền tảng của vắc xin Việt Nam.
Mới đây, Tạp chí Nature (Anh) đưa tin, Iran đã phê duyệt vắc xin được phát triển dựa trên cơ sở vắc xin tạo ra kháng thể trung hòa, mặc dù chưa làm xong giai đoạn 3, vì họ tin vào tính an toàn và khả năng bảo vệ tốt của vắc xin này.
Do đó, dựa trên bằng chứng tốt nhất hiện có (cân đối cẩn thận giữa rủi ro tiềm ẩn và lợi ích của sản phẩm dựa trên dữ liệu hiện có), Chính phủ có thể cấp phép sử dụng khẩn cấp đối với vắc xin Nanocovax, mà không cần phải chờ đợi tất cả bằng chứng cần thiết của giai đoạn 3.
“Việc sản xuất được vắc xin phòng Covid-19 có ý nghĩa vô cùng to lớn. Càng có được vắc xin sớm thì càng cứu sống được nhiều sinh mạng”, TS. Nguyễn Hữu Huân nhấn mạnh.
TS. Nguyễn Đức Thái (kiều bào Mỹ), đồng sáng lập chuỗi hội thảo thường niên Transmed-VN, cho rằng, để có thể cấp phép sử dụng khẩn cấp, vắc xin cần đạt được 4 tiêu chuẩn của Tổ chức Y tế thế giới (WHO), FDA (Hoa Kỳ) dựa trên kết quả lâm sàng là F0 không có triệu chứng, giảm nhập viện, giảm trở bệnh nặng, không tử vong. Ngoài ra, còn phải đáp ứng tốt đặc biệt cho chủng Delta, từ đó mới đo được hiệu năng của vắc xin. Tỷ lệ này có thể thay đổi theo từng loại vắc xin.
Theo TS. Nguyễn Đức Thái, Nanocovax cần đáp ứng tính đa dạng và phức tạp của cộng đồng dân số người Việt, số lượng 13 ngàn thử nghiệm là thấp nhất, nhu cầu khoa học là phải đánh giá trên số lượng lớn hơn. Nanocovax cũng cần bao phủ hơn về đối tượng (cao tuổi bệnh nền, tuyến đầu, quần chúng) và môi trường (vùng dịch, vùng xanh, vùng tiêm chủng) để vắc xin có giá trị tổng thể.
"Để đánh giá đúng hiệu quả theo chuẩn quốc tế, nhà sản xuất phải gia tăng số lượng thử nghiệm lâm sàng lên 30 - 50 ngàn người. Điều này là quá lý tưởng nhưng khó đáp ứng được ngay. Do vậy, nên dựa vào tính an toàn, tính sinh miễn dịch cộng đồng, khả năng bảo vệ để cho phép sử dụng, đối phó với trận chiến cam go hiện nay, từ đó xác định quần thể nào hiệu quả/không hiệu quả, dần dần mở rộng sử dụng tiêm chủng đại trà”, TS. Nguyễn Đức Thái đề xuất.
Từ kinh nghiệm trên thế giới, TS. Nguyễn Hữu Huân khuyến nghị, tại Việt Nam, có thể thành lập một hội đồng chuyên gia độc lập có tên tuổi, đầu ngành về vắc xin ở trong nước và trên thế giới (không có mối quan hệ về quyền lợi tài chính hay kỹ thuật) để cho ý kiến và bỏ phiếu thông qua. Cơ quan cấp phép sử dụng khẩn cấp sẽ dựa vào kết quả bỏ phiếu này để tham khảo, tự tin hơn khi phê duyệt. Hiện nay, tiêu chuẩn khoa học của Việt Nam còn nhiều hạn chế, nếu áp theo hệ thống tiêu chuẩn quốc tế thì khó khăn để phê duyệt. Do đó, Việt Nam nên sử dụng chuyên gia của Bộ Y tế và những người đã có kinh nghiệm phát triển vắc xin để chỉ ra khả năng bảo vệ, an toàn...
(Bài tuyên truyền thực hiện Nghị quyết 84/NQ-CP ngày 29/5/2020 của Chính phủ)







































